急性白血病免疫分型检测-流式细胞术应用(一)
急性白血病是起源于造血干细胞的恶性克隆疾病,发病时骨髓中异常的原始细胞及幼稚细胞(白血病细胞)大量增殖并抑制正常造血,可广泛浸润肝、脾、淋巴结等各种脏器。患者主要表现为贫血、出血、感染和浸润等症状。急性白血病可分为急性淋巴细胞白血病和急性髓系白血病两大类。
在我国急性淋巴细胞白血病的发病率约为0.69/10万人,较常见于儿童、青少年,急性髓系白血病约为1.62/10万人,较常见于成年人。急性白血病患者如果不接受系统正规的治疗,平均生存期仅3个月左右。并且治疗比较困难,且复发率比较高,大约有1/3的患者治疗达到完全缓解后会出现复发。不同类型的患者复发比例也并不相同,因为白血病的预后与白血病分型存在密切关系。
![]() 急性白血病免疫分型的临床意义
急性白血病免疫分型的临床意义
有助于正确鉴别急性白血病类型,可帮助临床医生选择最佳的治疗方案及对患者预后进行正确评估。
有助于临床医生根据预后将患者分为低危、中危、高危,可实现急性白血病的分层治疗。
有助于临床医生定期检测急性白血病患者微小残留病灶,可尽早发现疾病复发,从而对患者进行早期干预,提高急性白血病患者的无事件生存率。
![]() 急性白血病免疫分型的免疫标志选择
急性白血病免疫分型的免疫标志选择
流式细胞术诊断急性白血病常用标志分为基本免疫标志(表1)和可选标志(表2),并包括罕见类型如原始浆细胞样树突状细胞肿瘤。

资料来源于:中国中西医结合学会检验医学专业委员会. 急性白血病系别判断的流式细胞免疫分型专家共识[J]. 中华检验医学杂志,2021,44(12):1113-1125.
鉴于几乎没有任何标志是绝对敏感和特异的,做全标志有助于降低误诊风险,因此在系别筛查时如果出现系别标志表达过多或者过少,或者伴系表达标志的强度超过标本中残留的正常细胞时,首先应该做全两个诊断标准涉及的相关系别标志,必要时甚至需要增加CD371等新的髓系标志。在此过程中可以选择一步法或者两步法。选择一步法的实验室,以目前常用3激光8色机型为例,可供参考的5管法见表3;选择两步法的实验室,第一步进行系别筛查,包括髓系MPO(或者(CD33)和CD117,T系CD7和cCD3、B系CD19和CD22,根据采用仪器型号不同可能有差异,3激光8色推荐方案见表3。
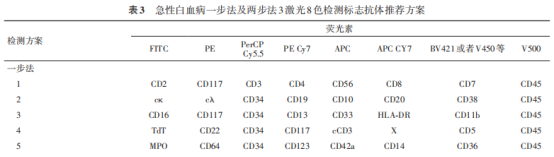

资料来源于:中国中西医结合学会检验医学专业委员会. 急性白血病系别判断的流式细胞免疫分型专家共识[J]. 中华检验医学杂志,2021,44(12):1113-1125.
![]() 推荐产品
推荐产品
巴德生物已完成几百种细胞标志物的荧光抗体试剂制备,种类涵盖了人淋巴细胞亚群分析、人调节T细胞分析、人间充质干细胞分析、人造血干细胞分析和阵发性血尿诊断等流式检测项目所涉及的抗体试剂。巴德的荧光抗体试剂具有以下优势:高度特异性;荧光选择丰富;荧光更亮更稳定。
|
巴德生物科技有限公司荧光抗体试剂清单 |
|||
|
名称 |
型号 |
规格 |
货号 |
|
CD4 |
APC-Cy7 |
50T/100T |
A00201003/A00201004 |
|
CD8 |
APC-Cy7 |
50T/100T |
A03801003/A03801004 |
|
CD14 |
APC-Cy7 |
50T/100T |
A00601003/A00601004 |
|
CD20 |
APC-Cy7 |
50T/100T |
A03301003/A03301004 |
|
CD3 |
APC |
50T/100T |
A00100203/A00100204 |
|
CD5 |
APC |
50T/100T |
A00300203/A00300204 |
|
CD10 |
APC |
50T/100T |
A03000203/A03000204 |
|
CD11c |
APC |
50T/100T |
A04800203/A04800204 |
|
CD33 |
APC |
50T/100T |
A01300203/A01300204 |
|
CD56 |
APC |
50T/100T |
A01800203/A01800204 |
|
CD79a |
APC |
50T/100T |
A05000203/A05000204 |
|
CD138 |
APC |
50T/100T |
A03700203/A03700204 |
|
CD303 |
APC |
50T/100T |
A06900203/A06900204 |
|
CD4 |
PE-Cy7 |
50T/100T |
A00200503/A00200504 |
|
CD13 |
PE-Cy7 |
50T/100T |
A03400503/A03400504 |
|
CD117 |
PE-Cy7 |
50T/100T |
A02600503/A02600504 |
|
CD2 |
PE |
50T/100T |
A06600103/A06600104 |
|
CD10 |
PE |
50T/100T |
A03000103/A03000104 |
|
CD22 |
PE |
50T/100T |
A00900103/A00900104 |
|
CD64 |
PE |
50T/100T |
A02000103/A02000104 |
|
CD117 |
PE |
50T/100T |
A02600103/A02600104 |
|
CD2 |
FITC |
50T/100T |
A06600903/A06600904 |
|
CD5 |
FITC |
50T/100T |
A00300903/A00300904 |
|
CD7 |
FITC |
50T/100T |
A00400903/A00400904 |
|
CD15 |
FITC |
50T/100T |
A01100903/A01100904 |
|
CD16 |
FITC |
50T/100T |
A03200903/A03200904 |
|
CD303 |
FITC |
50T/100T |
A06900903/A06900904 |
|
MPO |
FITC |
50T/100T |
A02900903/A02900904 |
![]() 参考文献
参考文献
[1]葛均波, 徐永健, 王辰. 内科学第9版[M]. 人民卫生出版社, 2018, 569-577.
[2]中国中西医结合学会检验医学专业委员会. 急性白血病系别判断的流式细胞免疫分型专家共识[J]. 中华检验医学杂志,2021,44(12):1113-1125.
[3]Patel SS, Weinberg OK. Diagnostic workup of acute leukemias of ambiguous lineage[J]. Am J Hematol, 2020, 95(6):718‑722.
[4]Arber DA, Orazi A, Hasserjian R, et al. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia[J]. Blood, 2016, 127(20):2391‑2405.
[5]Vardiman JW, Thiele J, Arber DA, et al. The 2008 revision of the World Health Organization (WHO) classification of myeloid neoplasms and acute leukemia: rationale and important changes[J]. Blood, 2009, 114(5):937-951.
[6]中国免疫学会血液免疫分会临床流式细胞术学组. 四色流式细胞术用于急性白血病免疫分型的中国专家共识(2015年版)[J]. 中华血液学杂志, 2015, 36(4):265-271.
Copyright © 2018 巴德生物科技有限公司 All Rights Reserved 备案号:沪ICP备xxxxxxxx号
地址:深圳市国家生物医药创新产业园1号楼东7层